Карбоновые кислоты и их химические свойства
 Химические соединения, основу которых составляет одна и более групп СООН, получили определение карбоновые кислоты.
Химические соединения, основу которых составляет одна и более групп СООН, получили определение карбоновые кислоты.
В основу соединений входит группа СООН, имеющая два составляющих — карбонил и гидроксил. Группу атомов СООН называют карбоксильной группой (карбоксилом). Взаимодействие элементов обеспечивается сочетанием двух атомов кислорода и атома углерода.
Оглавление:
Строение карбоновых кислот
Углеводородный радикал в одноосновных предельных кислотах соединяется с одной группой СООН. Общая формула карбоновых кислот выглядит так: R-COOH.
Строение карбоновой группы влияет на химические свойства.
Это интересно: анионы и катионы в химии, таблица растворимости.
Номенклатура
В названии карбоновых соединений сначала нумеруют атом углерода группы COOH. Количество карбоксильных групп обозначают приставками ди-; три-; тетра-.
Например,СН3-СН2-СООН — формула пропановой кислоты.
У карбоновых соединений существуют и привычные слуху названия: муравьиная, уксусная, лимонная…Все это названия карбоновых кислот.
Названия солей карбоновых соединений получаются из названий углеводорода с добавлением суффикса «-оат» (СООК)2- этандиот калия.
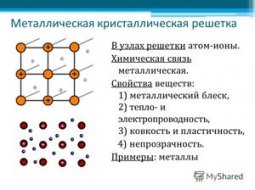
Это интересно: типы кристаллических решёток, таблица.
Классификация карбоновых кислот
Карбоновые кислоты классификация.
По характеру углеводорода:
- предельные;
- непредельные;
- ароматические.
По количеству групп СООН бывают:
- одноосновные (уксусная кислота);
- двуосновные (щавелевая кислота);
- многоосновные (лимонная кислота).
Предельные карбоновые кислоты — соединения, в которых радикал соединен с одним карбонилом.
Классификация карбоновых кислот разделяет их еще и по строению радикала, с которым связан карбонил. По этому признаку соединения бывают алифатические и алициклические.
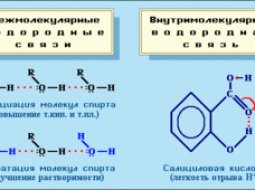
Это интересно: водородная связь образуется между молекулами, химический механизм.
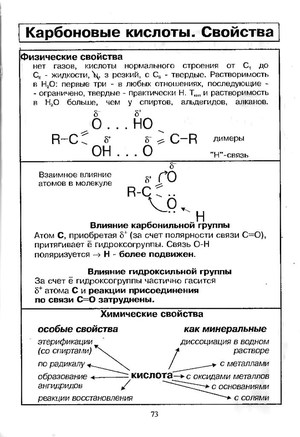
Физические свойства
 Рассмотрим карбоновые кислоты физические свойства.
Рассмотрим карбоновые кислоты физические свойства.
Карбоновые соединения имеют различное число атомов углерода. В зависимости от этого числа физические свойства этих соединений различаются.
Соединения, имеющие в составе от одного до трех углеродных атомов, считаются низшими. Это жидкости без цвета с резким запахом. Низшие соединения с легкостью растворяются в воде.
Соединения, имеющие в составе от четырех до девяти углеродных атомов — маслянистые жидкости, имеющие неприятный запах.
Соединения, имеющие в составе более девяти углеродных атомов, считаются высшими и физические свойства этих соединений таковы: они являются твердыми веществами, их невозможно растворить в воде.
Температура кипения и плавления зависит от молекулярной массы вещества. Чем больше молекулярная масса, тем выше температура кипения. Для закипания и плавления нужна более высокая температура , чем спиртам.
Получение карбоновых кислот
Существует несколько способов получения карбоновых кислот.
 Получение карбоновых соединений при помощи окисления спиртов. Спирты взаимодействуют с оксидом хрома и разбавленной серной кислотой с добавлением ацетона или марганцовки.
Получение карбоновых соединений при помощи окисления спиртов. Спирты взаимодействуют с оксидом хрома и разбавленной серной кислотой с добавлением ацетона или марганцовки.- При помощи окисления альдегидов (оксид хрома вступает в реакцию с оксидом серебра).
- При помощи окисления алкенов. Используют смесь перманганата калия и периодат натрия в водном растворе в нейтральной среде.
- При помощи окисления алкилбензолов получают ароматические кислоты.
- При помощи гидролиза.
- При помощи карбоксилирования металлсодержащих соединений.
- С помощью синтеза ароматических соединений.
- Выделение из природных веществ (например, из жиров).
- Получение карбоновых соединений возможно при омылении или гидролизе эфиров и спирта.
- Получение карбоновых соединений происходит и из цианидов при помощи нагревания.
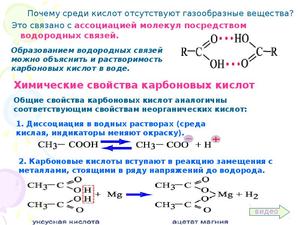
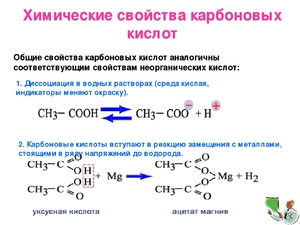
Химические свойства карбоновых кислот
При химических реакциях проявляются следующие свойства:
 диссоциация. Окрашивают лакмусовую бумажку в красный цвет, поскольку обладают кислыми свойствами;
диссоциация. Окрашивают лакмусовую бумажку в красный цвет, поскольку обладают кислыми свойствами;- вступая в реакции с металлами, солями, оксидами и гидроксидами водород замещается на активные металлы;
- при реакциях со спиртами гидроксил замещается на остаток спирта. Таким образом получается сложный эфир;
- всегда происходит замещение водорода на галогены;
- при взаимодействии с основными оксидами образуются соль и вода;
- при взаимодействии с гидроксидами образуются соли и вода;
Применение карбоновых кислот
Карбоновые соединения распространены в природе.Поэтому их применяют во многих областях: в промышленности (легкой и тяжелой), в медицине и сельском хозяйстве, а также в пищевой промышленности и косметологии.
Ароматические в большом количестве содержатся в ягодах и фруктах.
В медицине используют молочную, винную и аскорбиновую кислоту. Молочную применяют в качестве прижигания, а винную — как легкое слабительное. Аскорбиновая укрепляет иммунитет.
 В косметологии используются фруктовые и ароматические. Благодаря им клетки быстрее обновляются. Аромат цитрусовых способен оказать тонизирующее и успокаивающее действие на организм. Бензойная встречается в бальзамах и эфирных маслах, она хорошо растворяется в спирте.
В косметологии используются фруктовые и ароматические. Благодаря им клетки быстрее обновляются. Аромат цитрусовых способен оказать тонизирующее и успокаивающее действие на организм. Бензойная встречается в бальзамах и эфирных маслах, она хорошо растворяется в спирте.
Высокомолекулярные непредельные соединения встречаются в диетологии. Олеиновая в этой области наиболее распространена.
Полиненасыщенные с двойными связями (линолевая и другие) обладают биологической активностью. Их еще называют активными жирными кислотами. Они участвуют в обмене веществ, влияют на зрительную функцию и иммунитет, а также на нервную систему. Отсутствие этих веществ в пище или недостаточное их употребление затормаживает рост животных и оказывает негативное влияние на их репродуктивную функцию.
Сорбиновая получается из ягод рябины. Она является отличным консервантом.
Акриловая имеет едкий запах. Она применяется для получения стекла и синтетических волокон.
На основе реакции этирификации происходит синтез жира, который применяют при изготовлении мыла, а также моющих средств.
Муравьиная используется в медицине, в пчеловодстве, а также в качестве консервантов.
Уксусная — жидкость без цвета с резким запахом; легко смешивается с водой. Ее широко применяют в пищевой промышленности в качестве приправы. Также она используется при консервации. Еще она обладает свойствами растворителя. Поэтому широко применяется в производстве лаков и красок, при крашении. На ее основе изготавливают сырье для борьбы с насекомыми и сорняками.
Стеариновая и пальмитиновая (высшие одноосновные соединения) являются твердыми веществами и не растворяются в воде. Но их соли применяются в производстве мыла. Они делают брикеты мыла твердыми.
Поскольку соединения способны придавать однородность массам, то они широко используются в изготовлении лекарств.
Растения и животные также вырабатывают карбоновые соединения. Поэтому употреблять их внутрь безопасно. Главное, — соблюдать дозировку. Превышение дозы и концентрации ведет к ожогам и отравлениям.
Едкость соединений приносит пользу в металлургии, а также реставраторам и мебельщикам. Смеси на их основе позволяют выравнивать поверхности и очищать ржавчину.
Сложные эфиры, получаемые при реакции этерификации, нашли свое применение в парфюмерии. Они используются также в качестве компонентов лаков и красок, растворителей. А также как аромадобавки.
 Получение карбоновых соединений при помощи окисления спиртов. Спирты взаимодействуют с оксидом хрома и разбавленной серной кислотой с добавлением ацетона или марганцовки.
Получение карбоновых соединений при помощи окисления спиртов. Спирты взаимодействуют с оксидом хрома и разбавленной серной кислотой с добавлением ацетона или марганцовки. диссоциация. Окрашивают лакмусовую бумажку в красный цвет, поскольку обладают кислыми свойствами;
диссоциация. Окрашивают лакмусовую бумажку в красный цвет, поскольку обладают кислыми свойствами;




 1
1