Скорость химической реакции и факторы, на нее влияющие
 Механизмы протекания химических превращений и их скорости изучает химическая кинетика. Химические процессы протекают во времени с различными скоростями. Какие-то происходят быстро, почти мгновенно, для протекания других требуется весьма продолжительное время.
Механизмы протекания химических превращений и их скорости изучает химическая кинетика. Химические процессы протекают во времени с различными скоростями. Какие-то происходят быстро, почти мгновенно, для протекания других требуется весьма продолжительное время.
Оглавление:
- Факторы, способные влиять на скорость химической реакции
- Концентрация реагентов
- Природа реагентов
- Площадь поверхности соприкосновения реагентов
- Температура реакции
- Действие катализатора
- Давление
- Экспериментальное определение скорости химической реакции
- Тема видео: «Факторы, влияющие на скорость химической реакции.».
— как влияет природа реагирующих веществ?
— как влияет концентрация реагирующих веществ?
— как влияет температура на скорость химической реакции?
-что такое катализатор?
-что такое ферменты?
Скорость реакции — скорость с которой расходуются реагенты (их концентрация уменьшается) или образуются продукты реакции в единице объёма.
Это интересно: типы кристаллических решеток — таблица различных материалов.
Факторы, способные влиять на скорость химической реакции
На то, насколько быстро будет происходить химическое взаимодействие, могут повлиять следующие факторы:
- концентрация веществ;
- природа реагентов;
- температура;
- присутствие катализатора;
- давление (для реакций в газовой среде).
Таким образом, изменяя определённые условия протекания химического процесса, можно повлиять на то, насколько быстро будет протекать процесс.
Это интересно: металлы и неметаллы в периодической таблице Менделеева.
Концентрация реагентов
 В процессе химического взаимодействия частицы реагирующих веществ сталкиваются друг с другом. Количество таких совпадений пропорционально числу частиц веществ в объёме реагирующей смеси, а значит и пропорционально молярным концентрациям реагентов.
В процессе химического взаимодействия частицы реагирующих веществ сталкиваются друг с другом. Количество таких совпадений пропорционально числу частиц веществ в объёме реагирующей смеси, а значит и пропорционально молярным концентрациям реагентов.
Закон действующих масс описывает зависимость скорости реакции от молярных концентраций веществ, вступающих во взаимодействие.
Для элементарной реакции (А + В → …) данный закон выражается формулой:
υ = k ∙С A ∙С B,
где k — константа скорости; С A и С B — молярные концентрации реагентов, А и В.
Если одно из реагирующих веществ находится в твёрдом состоянии, то взаимодействие происходит на поверхности раздела фаз, в связи с этим концентрация твёрдого вещества не включается в уравнение кинетического закона действующих масс. Для понимания физического смысла константы скорости, необходимо принять С, А и С В равными 1. Тогда становится понятно, что константа скорости равна скорости реакции при концентрациях реагентов, равных единице.
Это интересно: как расставлять коэффициенты в химических уравнениях?
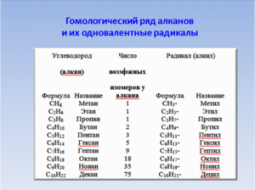
Природа реагентов
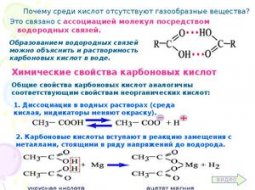
Так как в процессе взаимодействия разрушаются химические связи реагирующих веществ и образуются новые связи продуктов реакции, то большую роль будет играть характер связей, участвующих в реакции соединений и строение молекул реагирующих веществ.
Площадь поверхности соприкосновения реагентов
Такая характеристика, как площадь поверхности соприкосновения твёрдых реагентов, на протекание реакции влияет, порой, довольно значительно. Измельчение твёрдого вещества позволяет увеличить площадь поверхности соприкосновения реагентов, а значит и ускорить протекание процесса. Площадь соприкосновения растворимых веществ легко увеличивается растворением вещества.
Это интересно: водородная связь — примеры, механизм образования.
Температура реакции
 При увеличении температуры энергия сталкивающихся частиц возрастёт, очевидно, что с ростом температуры и сам химический процесс будет ускоряться. Наглядным примером того, как увеличение температуры влияет на процесс взаимодействия веществ, можно считать приведённые в таблице данные.
При увеличении температуры энергия сталкивающихся частиц возрастёт, очевидно, что с ростом температуры и сам химический процесс будет ускоряться. Наглядным примером того, как увеличение температуры влияет на процесс взаимодействия веществ, можно считать приведённые в таблице данные.
Таблица 1. Влияние изменения температуры на скорость образования воды (О 2 +2Н 2 →2Н 2 О)
| Температура, °С | Время |
| 18 | 230 млрд лет |
| 118 | 230 млн лет |
| 218 | 230 тыс. лет |
| 318 | 230 лет |
| 418 | 81 день |
| 518 | 2 ч. |
| 618 | 7 с. |
Для количественного описания того, как температура может влиять на скорость взаимодействия веществ используют правило Вант-Гоффа. Правило Вант-Гоффа состоит в том, что при повышении температуры на 10 градусов, происходит ускорение в 2−4 раза.
Математическая формула, описывающая правило Вант-Гоффа, выглядит следующим образом:
, где γ — температурный коэффициент скорости химической реакции (γ = 2−4).
Но гораздо более точно описывает температурную зависимость константы скорости уравнение Аррениуса:
, где R — универсальная газовая постоянная, А — множитель, определяемый видом реакции, Е, А — энергия активации.
Энергией активации называют такую энергию, которую должна приобрести молекула, чтобы произошло химическое превращение. То есть она является неким энергетическим барьером, который необходимо будет преодолеть сталкивающимся в реакционном объёме молекулам для перераспределения связей.
Энергия активации не зависит от внешних факторов, а зависит от природы вещества. Значение энергии активации до 40 — 50 кДж/моль позволяет веществам реагировать друг с другом довольно активно. Если же энергия активации превышает 120 кДж/моль, то вещества (при обычных температурах) будут реагировать очень медленно. Изменение температуры приводит к изменению количества активных молекул, то есть молекул, достигших энергии большей, чем энергия активации, а значит способных к химическим превращениям.
Действие катализатора
 Катализатором называют вещество, способное ускорять процесс, но не входящее в состав его продуктов. Катализ (ускорение протекания химического превращения) разделяют на · гомогенный, · гетерогенный. Если реагенты и катализатор находятся в одинаковых агрегатных состояниях, то катализ называют гомогенным, если в различных, то гетерогенным. Механизмы действия катализаторов разнообразны и достаточно сложны. Кроме того, стоит отметить, что для катализаторов характерна избирательность действия. То есть один и тот же катализатор, ускоряя одну реакцию, может никак не изменять скорость другой.
Катализатором называют вещество, способное ускорять процесс, но не входящее в состав его продуктов. Катализ (ускорение протекания химического превращения) разделяют на · гомогенный, · гетерогенный. Если реагенты и катализатор находятся в одинаковых агрегатных состояниях, то катализ называют гомогенным, если в различных, то гетерогенным. Механизмы действия катализаторов разнообразны и достаточно сложны. Кроме того, стоит отметить, что для катализаторов характерна избирательность действия. То есть один и тот же катализатор, ускоряя одну реакцию, может никак не изменять скорость другой.
Давление
Если в превращении участвуют газообразные вещества, то на скорость протекания процесса будет влиять изменение давления в системе. Это происходит потому, что для газообразных реагентов изменение давления приводит к изменению концентрации.
Экспериментальное определение скорости химической реакции
Определить быстроту протекания химического превращения экспериментально можно, получив данные о том, как в единицу времени меняется концентрация веществ, вступающих в реакцию, или продуктов. Методы получения таких данных делят на
- химические,
- физико-химические.
 Химические методы достаточно просты, доступны и точны. С их помощью скорость определяют, непосредственно замеряя концентрацию или количество вещества реагентов или продуктов. В случае медленной реакции, для контроля за тем, как расходуется реагент отбирают пробы. После чего определяют содержание в пробе реагента. Осуществляя отбор проб через равные промежутки времени, можно получить данные об изменении количества вещества в процессе взаимодействия. Чаще всего используют такие виды анализа, как титриметрия и гравиметрия.
Химические методы достаточно просты, доступны и точны. С их помощью скорость определяют, непосредственно замеряя концентрацию или количество вещества реагентов или продуктов. В случае медленной реакции, для контроля за тем, как расходуется реагент отбирают пробы. После чего определяют содержание в пробе реагента. Осуществляя отбор проб через равные промежутки времени, можно получить данные об изменении количества вещества в процессе взаимодействия. Чаще всего используют такие виды анализа, как титриметрия и гравиметрия.
Если реакция протекает быстро, то чтобы отобрать пробу, её приходится останавливать. Это можно сделать с помощью охлаждения, резкого удаления катализатора, также можно произвести разбавление либо перевести один из реагентов в не реакционноспособное состояние.
Методы физико-химического анализа в современной экспериментальной кинетике используются чаще, чем химические. С их помощью можно наблюдать изменение концентраций веществ в реальном времени. При этом реакцию нет необходимости останавливать и отбирать пробы.
Физико-химические методы основываются на измерении физического свойства, зависящего от количественного содержания в системе определённого соединения и изменяющегося со временем. Например, если в реакции участвуют газы, то таким свойством может быть давление. Также измеряют электропроводность, показатель преломления, спектры поглощения веществ.
Тема видео: «Факторы, влияющие на скорость химической реакции.».
— как влияет природа реагирующих веществ?
— как влияет концентрация реагирующих веществ?
— как влияет температура на скорость химической реакции?
-что такое катализатор?
-что такое ферменты?




 1
1 